Artículos Originales
Valoración de nuevos parámetros ecográficos en el diagnóstico del espectro de placenta acreta en la placenta previa
1Hospital Nacional Carlos Alberto Seguín Escobedo, Arequipa, Perú
2Universidad Nacional de San Agustín de Arequipa, Arequipa, Perú
3Hospital Rockingham Memorial, Sentara RMH Medical Center, Harrisonburg, VA 22801, USA
4Universidad Católica de Santa María, Arequipa, Perú
Determinar el acretismo de la placenta previa mediante las características anatómicas ecográficas y el perfil de la flujometría Doppler. Estudio descriptivo, prospectivo, de cohortes, longitudinal. Se usó la clasificación European Working Group on Abnormally Invasive Placenta (EW-AIP). Hospital Nacional del Sur de EsSalud, Arequipa, Perú. Gestantes de alto riesgo obstétrico (ARO) con diagnóstico de placenta previa, 20 a 40 semanas de gestación, diversa paridad y antecedente de cesárea. De 90 pacientes con diagnóstico de placenta previa de los años 2022 y 2023 se seleccionó 12 pacientes con sospecha de acretismo mediante valoración ecográfica y flujometría Doppler. La edad materna, el número de gestaciones, antecedente de legrado uterino, cesárea previa y mayor número de cesáreas tuvieron significación estadística, presentando la segunda y tercera cesárea 21,1 y 9,6 veces más riesgo de acretismo, respectivamente. Los criterios ecográficos fueron la pérdida de la zona clara, lagunas placentarias irregulares ovaladas, interrupción de la pared vesical, heterogeneidad e hiperecogenicidad placentaria, placa corial hiperecogénica e irregular, hipervasculatura de la pared vesical y subplacentaria, vasos nutricionales y lagunas placentarias hipervascularizadas. La velocidad máxima de flujo de 52,3 cm/ seg fue altamente significativa para acretismo placentario frente a 26,0 cm/seg en placentas previas sin signos de acretismo. La velocidad de flujo Doppler por encima de 50 cm/seg presentó mayor riesgo de acretismo y disminución de la sobrevida materna. En el estudio, los hallazgos ecográficos de a) heterogeneidad e hiperecogenicidad placentaria, b) placa corial hiperecogénica e irregular, y c) flujometría Doppler cuantificada con la velocidad máxima fueron útiles para predecir acretismo placentario.
Palabras clave: Placenta accreta; Placenta previa; corion; Ultrasonografía Doppler
INTRODUCCIÓN
El acretismo placentario es un problema obstétrico de salud pública que afecta la salud materna y neonatal. La evidencia nos demuestra que el PAS (placenta accreta spectrum) es una condición iatrogénica debida al incremento desmedido de las cesáreas 1,2).
Su fisiopatología no es conocida con certeza. Se describe que es producto de la implantación de la placenta en una zona anatómica del útero con alteración de los mecanismos celulares y moleculares, en zonas con decidualización deficiente o disfuncional o en una cicatriz previa incisional traumática de procedimientos como cesáreas, legrados uterinos o miomectomías 3,4).
El grado de invasión placentaria no depende de la edad gestacional 3). Pero, la implantación baja del saco gestacional en el segmento uterino inferior sobre una cicatriz de cesárea previa es la apariencia típica de acretismo placentario temprano. El grosor promedio del segmento uterino inferior en pacientes con cesárea previa puede llegar a 7 mm y los lagos vasculares anormales aparecen en el primer trimestre de gestación 4).
Los antecedentes personales y patológicos de la paciente son pilares de orientación para sospechar acretismo placentario, como la edad, multiparidad, número de cesáreas, miomectomías, legrados uterinos, retención placentaria e infecciones intramnióticas 4-6).
El diagnóstico temprano y su referencia a hospitales de alta complejidad podrían prevenir situaciones catastróficas por el manejo multidisciplinario de este estado mórbido. La valoración ecográfica temprana permite orientar el diagnóstico al identificar pérdida del espacio claro o línea hipoecogénica retroplacentaria, adelgazamiento e irregularidad de la pared del segmento en una zona de cicatriz previa, la presencia de lagunas vasculares intraplacentarias, hipervascularidad y el aumento de flujo en estas zonas defectuosas 4,6,7).
El problema del acretismo placentario surge cuando la placenta implantada anormalmente es separada forzadamente de la pared uterina, condicionando morbimortalidad materna potencial por hemorragias masivas, politransfusión sanguínea, rotura uterina, lesión de órganos adyacentes (vejiga, uréter, intestino, estructuras neurovasculares del retroperitoneo) y prematuridad. Se incrementa el riesgo de histerectomía y triplica el riesgo de perdidas hemáticas 4,6).
El objetivo del presente trabajo ha sido determinar el acretismo en placenta previa mediante las características anatómicas ecográficas y el perfil de flujometría Doppler.
MATERIALES Y MÉTODOS
El presente estudio fue de tipo descriptivo, prospectivo y longitudinal realizado en el Hospital Carlos Alberto Seguin Escobedo (HNCASE) de la Red Asistencial EsSalud de Arequipa Perú, entre enero 2021 y diciembre 2023. Se incluyeron gestantes de riesgo alto con diagnóstico de placenta previa referidos al hospital desde centros hospitalarios de menor complejidad de toda la zona sur del Perú (Arequipa, Moquegua, Tacna, y Puno).
Las gestantes con diagnóstico de placenta previa fueron evaluadas con ecografía y se hizo seguimiento hasta la culminación del embarazo. Las pacientes con sospecha de acretismo fueron programadas para cesárea e histerectomía, previa consejería y autorización de la paciente.
La valoración del acretismo se hizo según cuatro parámetros:
1. Historia clínica, mediante los antecedentes obstétricos de legrado o cesárea.
2. Hallazgos ecográficos basados en descriptores unificados sugeridos por The European Working Group on Abnormally Invasive Placenta (EW-AIP) 7), agregándose tres variables más en el presente estudio: a) heterogeneidad placentaria e hiperecogenicidad, b) placa corial de aspecto despulido, hiperecogénica e irregular, y c) flujometría Doppler cuantificada con la velocidad máxima. Se utilizó un ecógrafo Toshiba usxm-A500A, 2016.
3. Hallazgos intraoperatorios como la hipervascularidad del segmento y su grado de invasión a la vejiga, ausencia de plano de clivaje, imposibilidad de extracción manual completa de la placenta. 4. Resultados de anatomía patológica.
La paciente programada ingresó a sala de operaciones con sonda vesical número 18 de triple vía, previa interconsulta a Urología y con paquetes globulares en reserva. El procedimiento quirúrgico fue con incisión vertical mediana a 8 cm aproximadamente por debajo de la altura del apéndice xifoides hasta la altura de la sínfisis púbica, exposición de todo el cuerpo uterino gestante, incisión longitudinal fúndica de cuerpo uterino, extracción del producto, plicatura y sección del cordón umbilical sin tracción de la placenta, la cual quedó dentro de la cavidad uterina, histerorrafia de la zona cruenta fúndica y luego histerectomía según técnica convencional. En algunos casos se requirió la presencia del urólogo. En el postoperatorio inmediato, las pacientes pasaron a la unidad de cuidados intensivos debido a las alteraciones hemodinámicas y hematológicas.
RESULTADOS
Para el análisis, de una población total de 102 pacientes referidas con diagnóstico de placenta previa se seleccionaron 90 mujeres que reunieron los criterios de placenta previa, de las cuales 12 tuvieron los criterios ecográficos de sospecha de acretismo placentario. El acretismo mostró una incidencia del 13% para el presente trabajo.
La edad materna para placenta previa fluctuó entre 16 y 44 años y para acretismo placentario entre 25 y 37 años.
En la tabla 1 se observa la distribución de pacientes con riesgo de acretismo según edad, donde el 91,7% fueron mayores de 30 años y 8,3% de 30 años o menores.
Tabla 1 Antecedentes obstétricos relacionados al acretismo placentario con placenta previa.
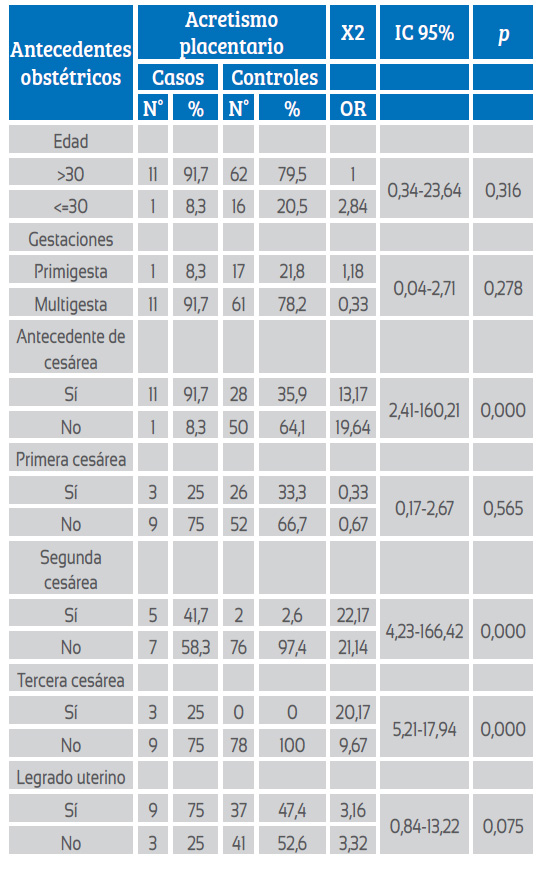
Según el número de gestaciones, el 8,3% de las pacientes que presentaron riesgo de acretismo fueron primigestas y 91,7% fueron multigestas.
El antecedente de cesárea previa en pacientes con riesgo de acretismo estuvo presente en 41,7%, con tres cesáreas 25%, y con antecedente de legrado uterino 75%.
Según el análisis, las gestantes con antecedente de segunda y tercera cesárea tuvieron 21,1 y 9,6 veces más riesgo de tener acretismo, respectivamente (p<0,05).
En la valoración ecográfica (tabla 2), la pérdida de la zona clara de la inserción placentaria para pacientes con sospecha de acretismo fue de 41,7%, había lagunas placentarias ovaladas no circulares de bordes irregulares en 75,0%, interrupción de la pared vesical en 50,0%, heterogeneidad e hiperecogenicidad placentaria en 66,7%, placa corial de aspecto despulido, hiperecogénica e irregular en 75%, hipervascularización uterovesical en 58,3%, hipervascularización subplacentaria en 50,0%, vasos nutricionales y lagunas placentarias hipervascularizadas en 66,7%, hipervasculatura intraplacentaria en 50%, y velocidad máxima de flujo de 52,3 cm/seg.
Tabla 2 Valoración ecográfica del acretismo placentario con placenta previa.
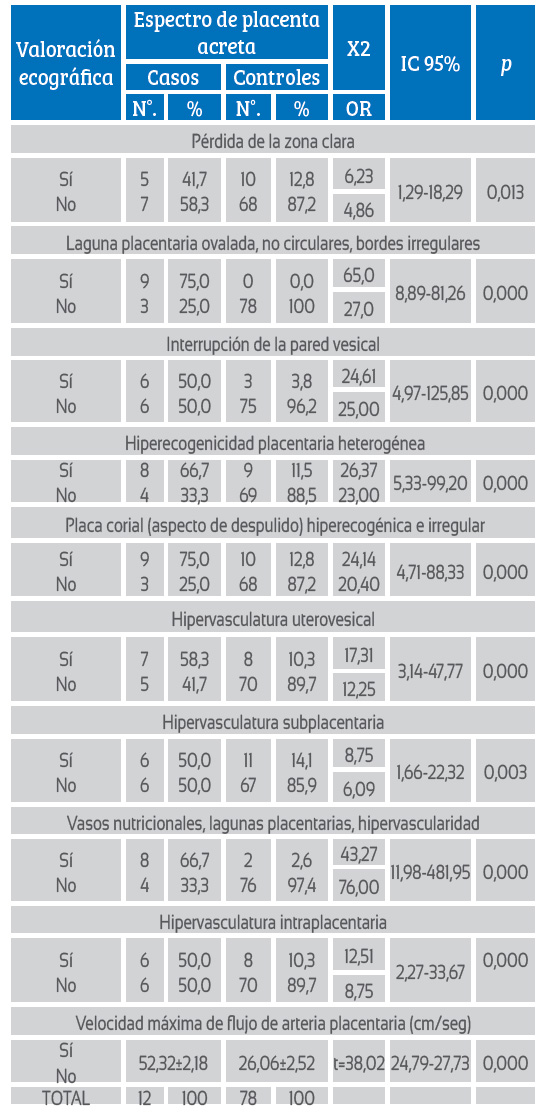
El análisis estadístico mostró que la pérdida de la zona clara, las lagunas placentarias ovaladas no circulares de bordes irregulares, la interrupción de la pared vesical, la hiperecogenicidad y heterogeneidad placentaria, la placa corial de aspecto despulido, hiperecogénica e irregular, la hipervascularización útero vesical así como la hipervascularización subplacentaria, vasos nutricionales e hipervascularización intraplacentaria presentaron relación estadísticamente significativa con el acretismo placentario (p<0,05). Y laflujometría representada por la velocidad máxima encontrada en el estudio Doppler con barrido de toda la placenta fue 52,3 para acretismo frente a 26,0 en placentas previas sin signos de acretismo, diferencia que fue estadísticamente significativa (p<0,05).
En la tabla 3 se muestra la regresión de Cox para el riesgo de acretismo y la supervivencia de las pacientes, donde se evidencia que las pacientes con una velocidad de hasta 53,4 cm/seg tuvieron un riesgo de acretismo de 1,0 con probabilidad de sobrevida de 33,3%. Sin embargo, las mujeres con una velocidad de flujo Doppler de 54,8 cm/seg presentaron incremento del riesgo de acretismo a 2,4 y la probabilidad de sobrevivencia disminuyó a 8,3%.
Tabla 3 Regresión de Cox para el riesgo de acretismo y la supervivencia de las pacientes.
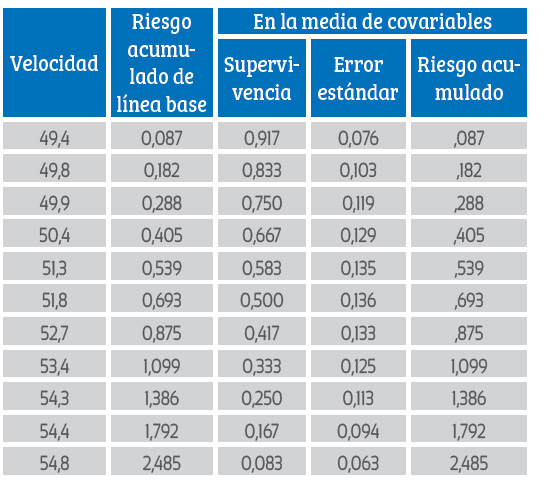
En la figura 1 se observa la regresión de Cox según la velocidad de flujo en relación con la supervivencia, en la que se ve que con una velocidad de flujo Doppler entre 40 y 50, el riesgo de acretismo es aproximadamente 1. Pero, si aumenta la velocidad de flujo Doppler a más de 50, la sobrevida disminuye (a más velocidad, la probabilidad de sobrevivir disminuye y el riesgo de acretismo aumenta).
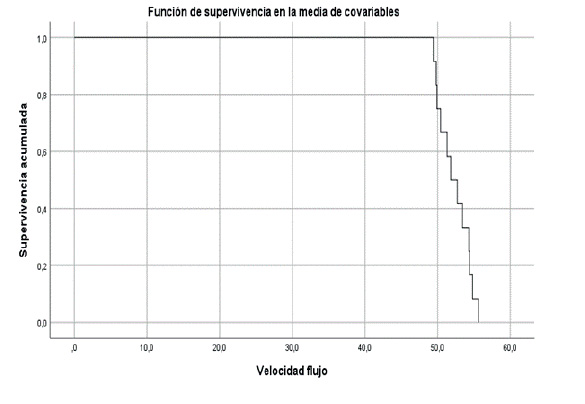
Figura 1 Diagrama con regresión de Cox, velocidad de flujo en relación con supervivencia.
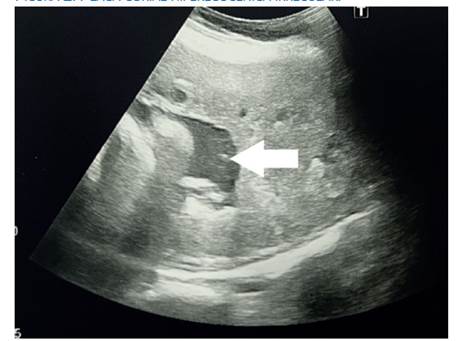
Figura 2 Placa corial hiperecogénica irregular.
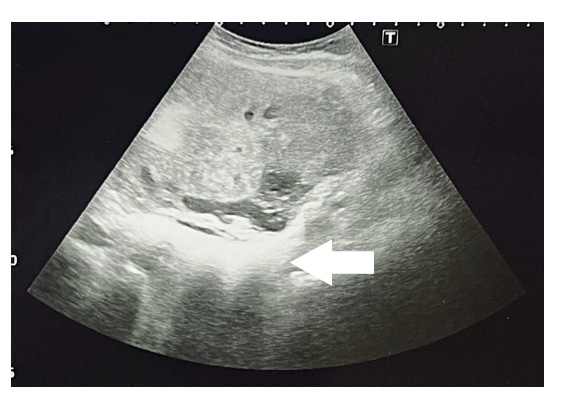
Figura 3 Hiperecogenicidad placentaria y heterogeneidad, hiperecogenicidad de placa corial.
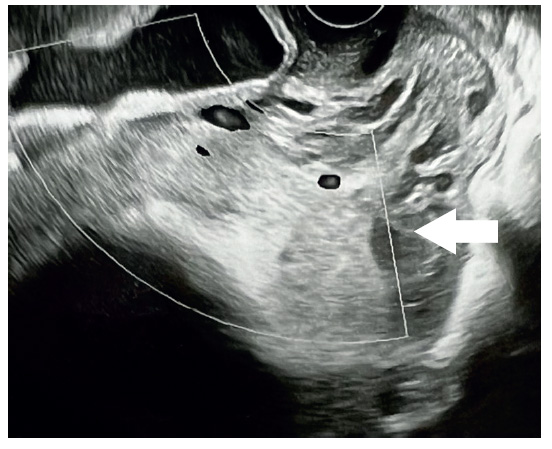
Figura 4.Lagunas placentarias ovaladas irregulares.
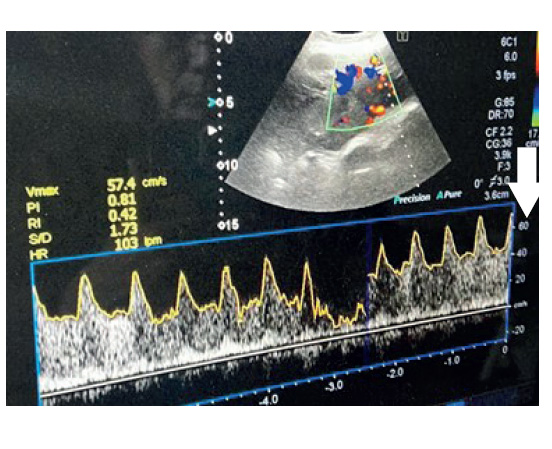
Figura 5 Medición de la flujometría Doppler.
DISCUSIÓN
El acretismo placentario es un evento multifactorial complejo, poco entendible, silencioso y asombroso por sus complicaciones sorpresivas que deterioran notablemente la salud materna y fetal con resultados deletéreos 8,9).
El acretismo está constituido por una placenta enferma desde su implantación, cuyas cualidades biomoleculares muestran características neoproliferativas similares al cáncer descritas por Weinberg y Hannahan. Entre ellas figuran la inducción de la angiogénesis 8,9), la señalización proliferativa sostenida 8,9), la resistencia a la muerte celular, la resistencia inmunológica 10,11). El procesamiento local de E-cadherina puede ser un mecanismo molecular importante que controla el fenotipo invasivo de la placenta acreta 12,13).
La placenta percreta presenta alteraciones de telómeros y cambios en la expresión de varios marcadores de senescencia que podrían estar relacionados con la maduración alterada de la invasión del trofoblasto 14). La incidencia del espectro de placenta acreta (placenta accreta spectrum - PAS) muestra un aumento progresivo en comparación a décadas pasadas 15 y su frecuencia es evidente en la práctica médica hospitalaria, consecuencia indudablemente iatrogénica y que en la actualidad es un problema de salud pública.
El diagnóstico ecográfico temprano marca la diferencia del pronóstico de estas pacientes. La pesquisa con una buena historia clínica y el diagnóstico ecográfico temprano determinan el pronóstico de estas pacientes 16).
Los hallazgos ecográficos más llamativos son la localización anormal de la placenta, hiperecogenicidad y heterogeneidad a la escala de grises en diversas zonas placentarias, parénquima placentario muy diferente al que estamos acostumbrados cuando observamos placentas normoinsertas 17). Por otro lado, se puede evidenciar modificaciones anatómicas de la placa basal y de la placa corial en la ecografía, producto de un proceso neoproliferativo que afecta toda la placenta en forma focal, parcial o total 18). Y la sombra que la acompaña es la presencia de lagunas vasculares de bordes irregulares, que no solamente tienen manifestaciones en la escala de grises sino, más bien, en el flujo aumentado en la placenta al medir con la flujometría Doppler. Estos hallazgos son sugerentes de acretismo 18,19).
La evidencia de los resultados muestra que, además de las variables utilizadas en el European Working Group on Abnormally Invasive Placenta (EW-AIP) 7), clasificación que tiene aproximadamente ocho años, las variables agregadas en nuestro estudio fueron tres: hiperecogenicidad placentaria y heterogénea, placa corial de aspecto de despulido e hiperecogénica irregular, y la velocidad máxima de flujo (cm/seg), que denotan una diferencia estadística significativa como aporte en el diagnóstico de acretismo. Por otro lado, se ha determinado el punto crítico de la flujometría placentaria como factor de riesgo de acretismo y pronóstico de sobrevida de las pacientes 18,19).
En el tratamiento del acretismo placentario existen diversas modalidades, incluyendo el conservador o el radical como la histerectomía, tratamientos que obedecen a las circunstancias individuales e idiosincrasia de las pacientes. El enfoque de tratamiento multidisciplinario estandarizado en pacientes con placenta mórbidamente adherente, que incluye accreta, íncreta y percreta, se asocia con menos morbilidad materna que cuando no se utiliza dicho enfoque 20). Indudablemente, el manejo de estas pacientes debe ser en hospitales de alta complejidad que cuenten con recursos de hemoderivados, banco de sangre, unidad de cuidados intensivos (UCI), entre otros. Pero, la regla de oro sigue siendo el diagnóstico precoz y la transferencia oportuna de estas pacientes, pues por su complejidad, el manejo debe ser multidisciplinario (21, 22).
Nuestro estudio presenta algunas limitaciones, como son en primer lugar el diseño retrospectivo realizado en un solo centro hospitalario, los registros médicos incompletos y el sesgo en la identificación de las historias clínicas con propensión a una inclinación de selección. En segundo lugar, las pacientes no fueron seleccionadas al azar y la información de referencia puede ser desequilibrada y sesgada. En tercer lugar, los signos ecográficos pueden verse afectados por factores humanos o técnicos. En cuarto lugar, el tamaño de la muestra fue pequeño, y no se analizaron los resultados del embarazo y los resultados neonatales de las pacientes.
CONCLUSIONES
La determinación ecográfica de la hiperecogenicidad placentaria heterogénea, placa corial hiperecogénica irregular (aspecto despulido) y la velocidad máxima del flujo Doppler (cm/seg) representan parámetros útiles de aporte al diagnóstico de acretismo placentario.
REFERENCIAS
1. Jauniaux E, Ayres-de-Campos D, Langhoff-Roos J, Fox KA, Collins S. FIGO classification for the clinical diagnosis of placenta accreta spectrum disorders. Int J Gynecol Obstet. 2019;146:20- 4. ORCID 10.1002/ijgo.12761 [ Links ]
2. Aguilera LR, Mojica-Palacios LM, Urquizu F, Gorena M, Tinajeros Guzmán F, Vergara Galliadi LM, Hidalgo A, Nieto-Calvache AJ. Difficulties in the Management of Placenta Accreta Spectrum in Hospitals with Limited Resources. Rev Bras Ginecol Obstet. 2022 May;44(5):467-74. doi: 10.1055/s-0042-1742408 [ Links ]
3. Garita Mendez E, Salas Morgan JP, Angulo Moya LC. Acretismo Placentario: Revisión bibliográfica. Rev Ciencia Salud Integrando Conocimientos. 2002;6(2):39-48. Doi: 10.34192/cienciaysalud.v6i2.390 [ Links ]
4. Véliz F, Núñez A, Selman A. Acretismo placentario: Un diagnóstico emergente. Abordaje quirúrgico no conservador. Rev Chilena Obstet Ginecol. 2018;83(5):513-26. Doi: 10.4067/s0717-75262018000500513 [ Links ]
5. Hernández Mendoza LD, Herrera Villalobos JE, Mendoza HF, Adaya Leythe EA. Acretismo placentario: Experiencia en Obstetricia Crítica. Rev Med UV. 2018;18(1):75-87. Doi: 10.25009/rmuv.2018.1.38 [ Links ]
6. Noguera SMF, Karchmer KS, Rabadán MCE, Sánchez PA. Acretismo placentario, un problema en aumento. El diagnóstico oportuno como éxito del tratamiento. Ginecol Obstet Mex. 2013;81(02):99-104. [ Links ]
7. Collins SL, Ashcroft A, Braun T, Calda P, Langhoff-Roos J, Morel O, Stefanovic V, Tutschek B, Chantraine F; European Working Group on Abnormally Invasive Placenta (EW-AIP). Proposal for standardized ultrasound descriptors of abnormally invasive placenta (AIP). Ultrasound Obstet Gynecol. 2016 Mar;47(3):271- 5. doi: 10.1002/uog.14952 [ Links ]
8. Muñiz Rizo ME, Álvarez Ponce VA, Felipe Cutié W. Acretismo placentario. Rev Cubana Obstet Ginecol [Internet]. 2015 Jun;41(2):190-6. http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0138- [ Links ]
9. Baltajian K, Hecht JL, Wenger JB, Salahuddin S, Verlohren S, Perschel FH, Zsengeller ZK, Thadhani R, Karumanchi SA, Rana S. Placental lesions of vascular insufficiency are associated with anti-angiogenic state in women with preeclampsia. Hypertens Pregn. 2014 Nov;33(4):427-39. doi: 10.3109/10641955.2014.926914 [ Links ]
10. Stanek J, Drummond Z. Occult placenta accreta: the missing link in the diagnosis of abnormal placentation. Ped Developm Pathol. 2007;10(4):266-73. doi: 10.2350/06-10-0174.1 [ Links ]
11. Bian Y, Xu X, Wang X, Zuo C, Meng J, Li H, Zhao S, et al. Downregulation of miR-29a/b/c in placenta accreta inhibits apoptosis of implantation site intermediate trophoblast cells by targeting MCL1. Placenta. 2016 Dec;48:13-9. doi: 10.1016/j.placenta.2016.09.017 [ Links ]
12. Ernst LM, Linn R, Minturn L, Miller E. Placental pathologic associations with morbidly adherent placenta potential insights into pathogenesis. Pediatr Dev Pathol. 2017 Sept-Oct;20:5:387-93. doi: 10.1177/1093526617698600 [ Links ]
13. Duzyj CM, Buhimschi IA, Motawea H, Laky CA, Cozzini G, Zhao G, Funai EF, Buhimschi CS. The invasive phenotype of placenta accreta extravillous trophoblasts associates with loss of E-cadherin. Placenta. 2015 Jun;36(6):645-51. doi: 10.1016/j.placenta.2015.04.001 [ Links ]
14. Tzadikevitch Geffen K, Gal H, Vainer I, Markovitch O, Amiel A, Krizhanovsky V, Biron-Shental T. Senescence and Telomere Homeostasis Might Be Involved in Placenta Percreta-Preliminary Investigation. Reprod Sci. 2018 Aug;25(8):1254-60. doi: 10.1177/1933719117737852 [ Links ]
15. Jauniaux E, Chantraine F, Silver RM, Langhoff-Roos J; FIGO Placenta Accreta Diagnosis and Management Expert Consensus Panel. FIGO consensus guidelines on placenta accreta spectrum disorders: Epidemiology. Int J Gynaecol Obstet. 2018 Mar;140(3):265-73. doi: 10.1002/ijgo.12407 [ Links ]
16. Horgan R, Abuhamad A. Placenta Accreta Spectrum: Prenatal Diagnosis and Management. Obstet Gynecol Clin North Am. 2022 Sep;49(3):423-38. doi: 10.1016/j.ogc.2022.02.004. [ Links ]
17. American College of Obstetricians and Gynecologists. Obstetric Care Consensus No. 7: Placenta accreta spectrum. Obstet Gynecol. 2018:132(6):e259-e275. https://doi.org/10.1097/AOG.0000000000002983 [ Links ]
18. Fratelli N, Prefumo F, Maggi C, Cavalli C, Sciarrone A, Garofalo A, et al. (Antenatal Diagnosis of Placental Adhesion Disorders) Working Group. Third-trimester ultrasound for antenatal diagnosis of placenta accreta spectrum in women with placenta previa: results from the ADoPAD study. Ultrasound Obstet Gynecol. 2022 Sep;60(3):381-9. doi: 10.1002/uog.24889. [ Links ]
19. Silver RM, Barbour KD. Placenta accreta spectrum: accreta, increta, and percreta. Obstet Gynecol Clin North Am. 2015 Jun;42(2):381-402. doi: 10.1016/j.ogc.2015.01.014 [ Links ]
20. Shamshirsaz AA, Fox KA, Salmanian B, Diaz-Arrastia CR, Lee W, Baker BW, et al. Maternal morbidity in patients with morbidly adherent placenta treated with and without a standardized multidisciplinary approach. Am J Obstet Gynecol. 2015 Feb;212(2):218.e1-9. doi: 10.1016/j.ajog.2014.08.019 [ Links ]
21. Lee PS, Kempner S, Miller M, Dominguez J, Grotegut C, Ehrisman J, et al. Multidisciplinary approach to manage antenatally suspected placenta percreta: updated algorithm and patient outcomes. Gynecol Oncol Res Pract. 2017 Aug 22;4:11.doi: 10.1186/s40661-017-0049-6 [ Links ]
22. Bailit JL, Grobman WA, Rice MM, Reddy UM, Wapner RJ, Varner MW, et al; Eunice Kennedy Shriver National Institute of Child Health and Human Development (NICHD) Maternal-Fetal Medicine Units (MFMU) Network. Morbidly adherent placenta treatments and outcomes. Obstet Gynecol. 2015 Mar;125(3):683-9. doi: 10.1097/AOG.0000000000000680 [ Links ]
Comments (0)